
發布時間:2019-12-30 來源:藥智網 浏覽量:73次
2019年,創新藥開(kāi)發依舊(jiù)火(huǒ)熱,國産1類新藥IND數量繼續超過110個,再創新高;正大(dà)天晴8件IND獲國家CDE受理,位列所有國内藥企之首,緊随其後為石藥集團、廣東東陽光、江蘇恒瑞等;所有IND基本信息及部分(fēn)品種披露信息見本稿。
1. 2019全年:國産1類新藥IND總體(tǐ)情況
2019全年,國産1類新藥(化藥)注冊申報IND品種>110個(2018年近于100個),創新品種開(kāi)發形勢整體(tǐ)處于增長趨勢。
其中(zhōng),全年注冊申報數量最多的月份為1月,共16個品種進入IND階段,最少的月份為9月,國産1類新藥IND僅1個品種(PS:為體(tǐ)現國産1類新藥創新水品,外(wài)國企業注冊申報的進口IND不列入統計之内)。
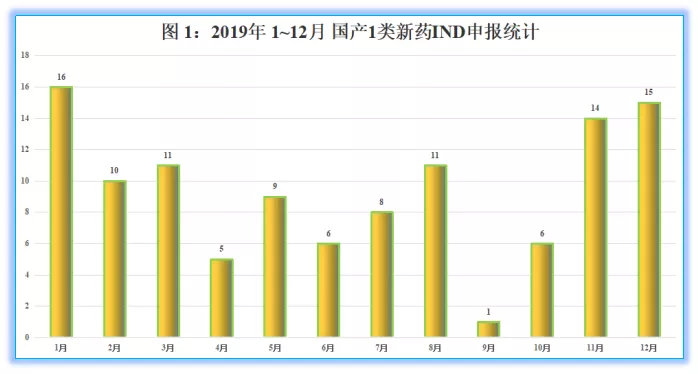
2. 2019全年:國産1類新藥IND企業分(fēn)析
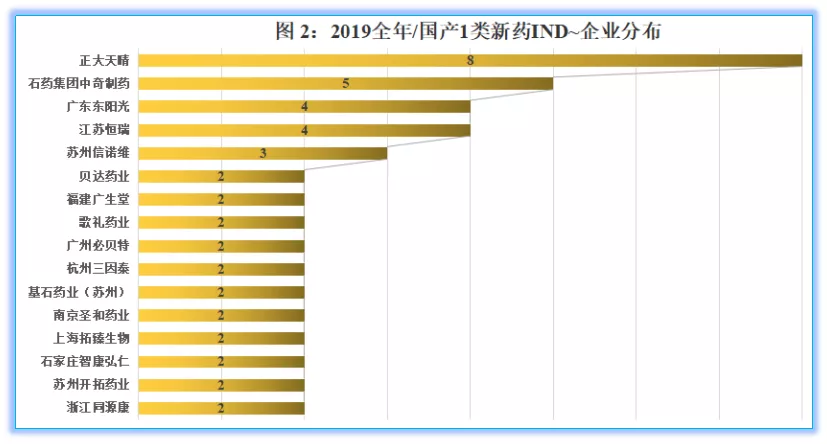
企業方面,IND申報數量相對較多的為正大(dà)天晴,共8件,品種分(fēn)别為TQB3562片、TQA3563片、TQB3804片、TQC3564片、TQB3303片、TQB3602膠囊、TQB3473片、TQB3728片;天晴對于IND申報品種所對外(wài)披露的信息相對不多,這些品種的具體(tǐ)方向和特點需要進一(yī)步等待公司披露。
緊随正大(dà)天晴之後的為石藥集團中(zhōng)奇制藥(5件)、廣東東陽光(4件)、江蘇恒瑞(4件)、蘇州信諾維(3件);IND品種數量為2個的企業還有浙江同源康、蘇州開(kāi)拓藥業、石家莊智康弘仁、上海拓臻生(shēng)物(wù)、南(nán)京聖和藥業、基石藥業(蘇州)、杭州三因泰、廣州必貝特、歌禮藥業、福建廣生(shēng)堂、貝達藥業。
3. 2019全年:國内部分(fēn)IND品種分(fēn)析
新藥IND階段的品種,由于種種原因,披露的信息往往不多,通過查詢,部分(fēn)IND品種信息如下(xià),排列順序為時間倒序。
CS3002
由基石藥業開(kāi)發,為CDK4/6選擇性抑制劑,通過特異性抑制CDK4/6激酶的活性,達到抑制腫瘤生(shēng)長的目的。臨床前研究表明,CS3002具有與palbociclib相當的體(tǐ)内外(wài)活性,在小(xiǎo)鼠動物(wù)模型中(zhōng),聯合PD-1單抗或内分(fēn)泌治療均顯示出了良好的抑制腫瘤生(shēng)長的作用,且聯合治療優于單藥治療;在安全性及耐受性上也顯示出潛在優勢。
PS:已收到澳大(dà)利亞人類研究倫理委員(yuán)會簽發的臨床試驗倫理許可。
ABSK011
由上海和譽生(shēng)物(wù)醫藥科技有限公司開(kāi)發,為公司獨立自主研發的小(xiǎo)分(fēn)子口服FGFR4抑制劑,其優良的活性、選擇性及其它理化特性預示着該藥物(wù)具有成為全球best-in-class潛力,該藥物(wù)的臨床開(kāi)發将進一(yī)步拓寬和譽醫藥在腫瘤治療領域的布局。
PS:已獲得台灣食品藥品監督管理局臨床試驗許可,即将開(kāi)展針對肝細胞癌的臨床1期研究。
GST-HG131
由福建廣生(shēng)堂藥業股份有限公司開(kāi)發,是擁有全球知(zhī)識産權的乙肝治療全球創新藥,屬First-in-Class全球領先項目,有機會成為全球首個上市的乙肝HBsAg抑制劑創新藥,是公司乙肝功能性治愈“登峰計劃”重要組合方案之一(yī)。GST-HG131核心化合物(wù)已申請PCT國際專利,其中(zhōng)國專利已獲得授權通知(zhī)書(shū)。
BPI-27336
由貝達藥業自主研發的擁有完全自主知(zhī)識産權的新分(fēn)子實體(tǐ)化合物(wù),是一(yī)種新型強效、選擇性的細胞外(wài)調節激酶1/2(ERK1/2)口服小(xiǎo)分(fēn)子抑制劑,拟用于RAS/RAF/MEK激活變異的結直腸癌、胰腺癌、肺癌、肝癌、胃癌、黑色素瘤等實體(tǐ)瘤的治療。截至公告披露日,全球範圍内尚無ERK1/2抑制劑上市,國外(wài)有若幹ERK1/2抑制劑處于臨床研究階段。
HH2710
由上海海和藥物(wù)與中(zhōng)國科學院上海藥物(wù)研究所合作開(kāi)發,是一(yī)種高效、特異性的小(xiǎo)分(fēn)子ERK激酶抑制劑。早期的非臨床研究結果顯示,HH2710的體(tǐ)外(wài)抗腫瘤活性、藥代動力學特性及安全性表現俱佳;在CDX模型中(zhōng),HH2710的體(tǐ)内抗腫瘤活性明顯優于相同劑量下(xià)的同類化合物(wù)。且2019年09月,已獲得美國FDA的臨床試驗許可,拟用于治療經檢測确認存在MAPK信号通路基因異常的惡性腫瘤。
KC1036
KC1036是康辰藥業自主研發的境内外(wài)均未上市的化學藥品1類創新藥,拟用于實體(tǐ)腫瘤和血液腫瘤的治療。屬多靶點酪氨酸激酶抑制劑,臨床前研究結果顯示,KC1036激酶活性強,在多種實體(tǐ)腫瘤和血液腫瘤的動物(wù)模型中(zhōng)均表現出顯著抑瘤活性,且安全性較好。康辰藥業稱,截至公告日,公司在KC1036項目上投入的研發費(fèi)用約2277萬元。
ORIN1001
ORIN1001是複星醫藥子公司“複星弘創”自主研發的具有新酶型靶點、新作用機制和新化學結構類型的首創(First-in-Class)小(xiǎo)分(fēn)子藥物(wù),用于治療晚期實體(tǐ)瘤,其第一(yī)個探索中(zhōng)的适應症為複發性、難治性、轉移性乳腺癌。截至2019年5月,複星醫藥集團針對該新藥已累計投入為約4547萬元用于研發。且美國FDA已授予其新藥ORIN1001用于治療複發性、難治性、轉移性乳腺癌(包括三陰乳腺癌)的快速通道資(zī)格(Fast Track designation)。
FCN-647
複星醫藥控股子公司重慶複創醫藥研究有限公司開(kāi)發,用于治療複發或難治的B淋巴細胞惡性腫瘤,截至2019年9月,該集團現階段針對該新藥累計研發投入為人民币約2368萬元(未經審計)。根據IQVIA數據,與該新藥同靶點的藥品在全球的銷售額約為45.1億美元。
HSK21542
由海思科開(kāi)發,為全新具有自主知(zhī)識産權的鎮痛藥物(wù),拟用于急慢(màn)性疼痛的治療,注冊分(fēn)類為化藥1類。據臨床前研究,HSK21542為外(wài)周kappa阿片受體(tǐ)的選擇性激動劑,具有強效且長效的鎮痛作用,不易透過血腦屏障,在發揮外(wài)周鎮痛的同時,能避免中(zhōng)樞阿片類藥物(wù)相關副作用,如成瘾、緻幻、呼吸抑制等。這些特點表明HSK21542具有藥效顯著、安全性良好等明顯臨床優勢,可為衆多的急慢(màn)性疼痛患者提供更優的用藥選擇。截至目前,公司在HSK21542注射液的研發投入約2,000萬元。
SH2442
由南(nán)京聖和藥業股份有限公司自主開(kāi)發,是一(yī)款乙酰輔酶A羧化酶的小(xiǎo)分(fēn)子抑制劑,為國内首家申報的該靶點創新藥,用于治療非酒精性脂肪性肝炎(NASH)及其引起的肝纖維化,擁有貝諾司他化合物(wù)、合成工(gōng)藝、制劑、用途的全球知(zhī)識産權。
TY-302
由鄭州泰基鴻諾醫藥股份有限公司開(kāi)發,擁有完全自主知(zhī)識産權,是一(yī)種強效、高選擇性的口服細胞周期蛋白(bái)依賴性激酶4/6(CDK4/6)抑制劑,用于激素受體(tǐ)陽性和表皮生(shēng)長因子受體(tǐ)2陰性(HR+/HER2-)局部晚期或轉移性乳腺癌等晚期實體(tǐ)瘤或血液系統腫瘤的治療。2019年10月份以來,由該公司自主研發的抗肺癌新藥和抗乳腺癌藥物(wù)兩個國家1.1類新藥項目相繼獲得臨床試驗批準。
GST-HG141
福建廣生(shēng)堂藥業股份有限公司曆經四年完成了GST-HG141申請臨床試驗所需的全部數據和全套資(zī)料,于2019年8月收到國家藥品監督管理局下(xià)發的《受理通知(zhī)書(shū)》,公司乙肝治療全球創新藥乙肝核心蛋白(bái)抑制劑GST-HG141臨床申請獲得受理,申請階段“臨床”。該項目是廣生(shēng)堂在衆多基礎研究科學家指導下(xià)提出的乙肝功能性治愈“登峰計劃”的最重要組成藥物(wù)之一(yī),是與具備領先新藥研發實力的上海藥明康德新藥開(kāi)發有限公司合作研發的成果,目前全球尚無該靶點藥物(wù)上市,有望成為Best-in-class項目。目标:挑戰乙肝功能性治愈。GST-HG141核心化合物(wù)已申請PCT國際專利,計劃進入中(zhōng)國、美國、日本、歐洲等24個國家和地區。
HTD1801
HTD1801,由深圳君聖泰生(shēng)物(wù)開(kāi)發,FDA已授予其研究性小(xiǎo)分(fēn)子創新藥HTD1801治療非酒精性脂肪性肝炎(NASH)的快速通道審評資(zī)格認定。之前,FDA還授予了HTD1801治療原發性硬化性膽管炎(PSC)的孤兒藥資(zī)格認定和快速通道審評資(zī)格認定。目前,HTD1801治療PSC的II期臨床試驗正在美國開(kāi)展,治療NASH的II期研究計劃很快在美國啟動患者招募。
TY-9591
同源康醫藥首個進入臨床試驗的國家1類抗腫瘤靶向新藥,第三代表皮生(shēng)長因子受體(tǐ)(EGFR)抑制劑,對标奧希替尼,其化合物(wù)發明專利已獲授權。
DN1508052-01
上海迪諾醫藥開(kāi)發,一(yī)種高效的小(xiǎo)分(fēn)子TLR8激動劑(國内提交IND的首個TLR8激動劑),拟用于癌症的免疫治療。2018年11月,上海迪諾醫藥收到FDA已完成DN1508052-01新藥臨床研究申請(IND)審核的信函。2019年5月下(xià)旬,上海迪諾醫藥啟動了一(yī)項開(kāi)放(fàng)、多中(zhōng)心的Ⅰ期臨床試驗,拟招募25名受試者,旨在初步評價DN1508052-01單藥經皮下(xià)注射用于實體(tǐ)瘤患者的安全耐受、藥物(wù)代謝動力學特性及抗腫瘤活性。
JAB-3312
JAB-3312可以阻斷KRAS-MAPK信号通路,用于治療非小(xiǎo)細胞肺癌、結直腸癌、胰腺癌等實體(tǐ)瘤,同時也可以解除腫瘤免疫抑制微環境,增強現有腫瘤免疫療法的功效。2019年7月3日,加科思自主開(kāi)發的小(xiǎo)分(fēn)子口服JAB-3312獲得美國FDA新藥臨床試驗許可,這是繼JAB-3068進入臨床IIa期之後,公司第二個進入臨床的小(xiǎo)分(fēn)子抗癌藥。
富馬酸奧比特嗪
富馬酸奧比特嗪,由中(zhōng)南(nán)大(dà)學和深圳市真興醫藥技術有限公司合作開(kāi)發,能特異性激活腫瘤細胞凋亡信号轉導通路關鍵酶原~半胱天冬蛋白(bái)酶-3酶原,将其活化為腫瘤凋亡關鍵執行分(fēn)子半胱天冬酶-3,而導緻腫瘤細胞快速死亡。臨床适應症主要為非小(xiǎo)細胞肺癌。
TERN-201
TERN-201,最初由禮來(Eli Lilly)研發。2018年,拓臻生(shēng)物(wù)與禮來簽訂開(kāi)發、制造和商(shāng)業化TERN-201治療NASH的全球獨家協議。在2019上半年于維也納舉行的國際肝髒大(dà)會上,拓臻生(shēng)物(wù)發表了TERN-201臨床前研究數據,顯示其在NASH齧齒類動物(wù)模型中(zhōng)顯著改善肝髒NAS評分(fēn)和纖維化。拓臻生(shēng)物(wù)最近自GENFIT獲得在大(dà)中(zhōng)華區開(kāi)發、制造和商(shāng)業化PPAR α/δ 雙重激動劑Elafibranor用于治療非酒精性脂肪性肝炎(NASH)和原發性膽汁性膽管炎(PBC)的專有權。Elafibranor前期臨床試驗結果顯示針對NASH和PBC兩種适應症的正面結果,并有可能成為未來聯合用藥療法的重要組成部分(fēn)。
AST-3424
AST-3424是艾欣達偉和台灣浩鼎聯合研發的一(yī)款以過表達AKR1C3為标靶的first-in-class抗癌藥。AST-3424在AKR1C3作用下(xià),會選擇性地釋出強效DNA烷基化劑,啟動殲滅癌細胞機制;這種選擇性啟動機制,使得AKR1C3在多種抗藥性及難治癌症,如肝癌,去(qù)勢抵擋性前列腺癌,T細胞急性淋巴性白(bái)血病等腫瘤細胞中(zhōng),均有高度表現。台灣浩鼎正在美國進行治療實體(tǐ)瘤的臨床I/II期研究。2018年7月,OBI-3424獲得FDA孤兒藥資(zī)格。2019年4月,NMPA受理本品的臨床試驗申請。
TSL-0319
TSL-0319膠囊是天士力自主研發的二肽基肽酶4(DPP-4)抑制劑,通過抑制胰高血糖素樣肽-1(GLP-1)和葡萄糖依賴性促胰島素分(fēn)泌多肽(GIP)的滅活,促進胰島釋放(fàng)胰島素,從而提高胰島素水平,達到降低血糖的目的。該藥屬于1類化學藥,擁有完全自主知(zhī)識産權,屬于境内外(wài)均未上市的創新藥。該項目目前已投入研發費(fèi)用約1694.65萬元。
注射用LH021
LH021具有潛在的修複膝關節受損軟骨的特點,屬于改善病情藥物(wù)。
2015~2016年,完成了機制研究;
2016年5月,正式立項;6月,啟動藥學CMC;12月,申請國内專利;
2017年6月,啟動安評研究;
2018年9月,IND package正式完成;10月召開(kāi)pre-IND meeting;
2019年1月,正式提交IND;3月正式受理。臨床試驗方案設計的思路将主要借鑒國外(wài)DMOAD類藥物(wù)臨床研究的經驗。
參考國内外(wài)同類産品的臨床試驗經驗,LH021首次人體(tǐ)I期臨床試驗的受試者人群将選擇符合入選标準的原發性膝骨關節炎患者,而不選擇健康受試者。I期臨床試驗除了考察LH021劑量爬升過程的耐受性和藥代特點,同時也将探索LH021的劑量跟療效以及軟骨合成和代謝相關生(shēng)物(wù)标記物(wù)的關系,為II期臨床試驗給藥方案的制定提供依據。
首次人體(tǐ)臨床試驗采用單次聯合多次劑量遞增給藥用于治療原發性膝關節骨關節炎。單次給藥後觀察28天,多次給藥一(yī)周期後随訪28天,試驗周期共計11周。
TTP273
TTP273,是vTv公司利用其小(xiǎo)分(fēn)子藥物(wù)研發平台發現的非肽類、高選擇性胰高血糖素樣肽-1受體(tǐ)(GLP-1r)激動劑,為vTv公司全球首創(first-in-class),目前在美國已完成IIb期臨床研究,結果顯示TTP273對降低糖尿病患者的糖化血紅蛋白(bái)效果明顯,且耐受性良好。TTP273項目最大(dà)的特色和亮點在于目前上市的GLP-1及其類似物(wù),均為注射劑型,而TTP273産品為首創的小(xiǎo)分(fēn)子非肽類口服劑型。中(zhōng)美華東本次通過授權許可形式引入TTP273項目,并作為公司在GLP-1類糖尿病産品線的補充,與公司現有在研的利拉魯肽注射液形成優勢互補。
101BHG-D01
101BHG-D01,為北(běi)京碩佰醫藥科技有限責任公司開(kāi)發的用于治療哮喘/慢(màn)阻肺的1類新藥。北(běi)京碩佰醫藥科技有限責任公司,于2016年在北(běi)京市豐碩維康技術開(kāi)發有限責任公司(2001年成立)和北(běi)京嘉事聯博醫藥科技有限公司(2007年成立)基礎上,經融資(zī)重組而設立。公司共有研發團隊40人,核心團隊具有30多年的新藥研發經驗,分(fēn)設藥學部、臨床醫學部、行政人事部、知(zhī)識産權部等部門,主要經營業務是創新藥物(wù)研發。
LH021
LH021,為廣州領晟醫療科技有限公司自主研發的用于治療骨關節炎的1類新藥。廣州領晟醫療科技有限公司成立于2012年,從事新靶點創新藥物(wù)研發,公司由海外(wài)留學人員(yuán)和國内醫藥行業精英創立,目前公司的研發管線中(zhōng)已有12個新藥項目,覆蓋腫瘤、消化科等重大(dà)的慢(màn)性疾病領域以及老齡化相關的專科疾病。
GST-HG151
GST-HG151,為福建廣生(shēng)堂藥業股份有限公司與上海藥明康德新藥開(kāi)發有限公司合作研發的非酒精性脂肪肝病及肝纖維化可逆轉藥物(wù)。臨床前研究展示了改善肝功能 的作用和顯著的抗纖維化效果,有望填補全球抗肝纖維化領域的空白(bái),攻克肝纖維化、肝硬化不可逆轉的世界性難題。
LX-039
LX-039,為山東羅欣藥業集團股份有限公司開(kāi)發的乳腺癌領域1類新藥,該藥物(wù)是新型的、口服有效的選擇性雌激素受體(tǐ)下(xià)調劑,将主要用于晚期乳腺癌的治療。目前,國内外(wài)尚無該機理口服藥物(wù)上市,同類産品處于臨床I/II期。
YPS345
YPS345,為天方藥業有限公司與中(zhōng)國科學院生(shēng)物(wù)物(wù)理研究所共同開(kāi)發的拟用于腫瘤患者胸部放(fàng)射治療引起的肺炎、肺纖維化治療的1類新藥,目前市場尚無相同産品。天方藥業在開(kāi)展YPS345非臨床試驗研究階段,經有效性及安全性研究結果表明,作為預防和治療放(fàng)射性炎症的藥物(wù),其對動物(wù)模型上放(fàng)化療誘導的肺纖維化均有顯著的緩解作用,且安全性好。
CS3003
CS3003,為基石藥業開(kāi)發的HDAC6選擇性抑制劑,可作為單藥治療也可與常規标準療法聯用,有在多發性骨髓瘤中(zhōng)展示更好的療效的潛力。臨床前研究數據以及同類産品的臨床前和早期臨床研究還發現,CS3003較廣譜HDAC抑制劑可能具備更好的安全性,以及有在不同的适應症中(zhōng)開(kāi)發與免疫檢查點抑制劑聯合治療的潛力。
ASC21
ASC21,由歌禮制藥開(kāi)發,是一(yī)種與NS5B聚合酶結合的核苷酸抑制劑,通過抑制NS5B聚合酶的活性從而阻止慢(màn)性丙肝病毒感染。臨床前研究表明,ASC21是一(yī)種有效的泛基因型藥物(wù),耐藥基因屏障高。歌禮計劃将其與拉維達韋聯用,用于治療難治型、肝硬化及HCV/HIV共感染的患者。
附表:2019全年國内1類新藥IND數據
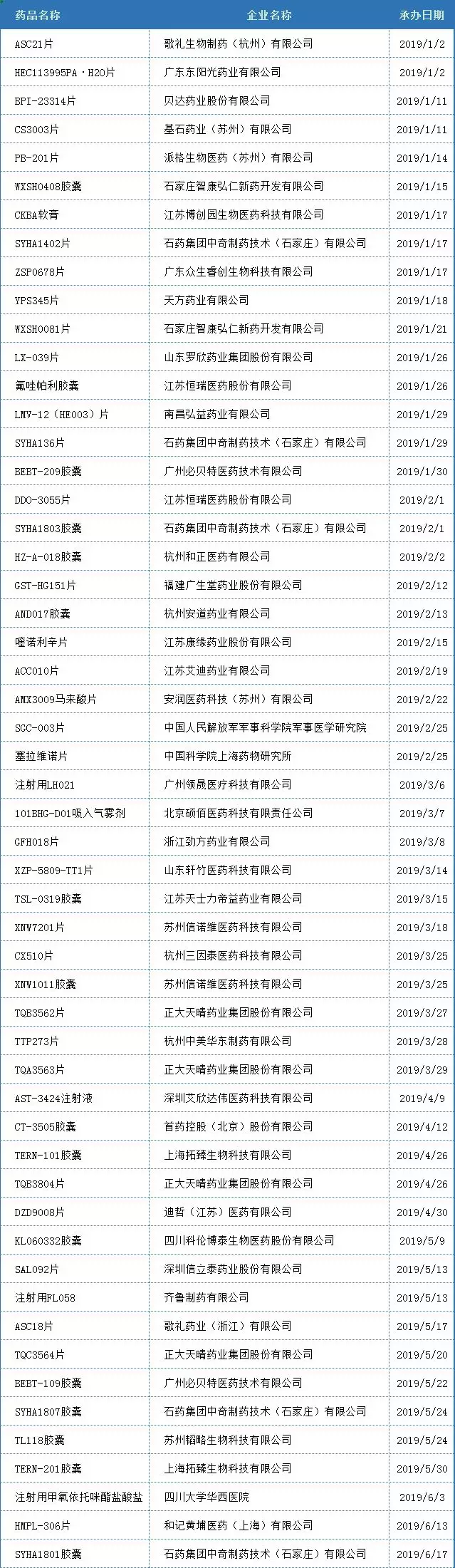
(以品種首次承辦日期統計,國外(wài)企業不列入統計範圍;統計時間2019.12.26)
數據來源:藥智數據、受理公告、雪球、搜狐醫藥、新浪醫藥、各大(dà)公司官網(及《受理通知(zhī)書(shū)》公告)、證券公司官網。
聯系我(wǒ)(wǒ)們
服務熱線:028-87988946 、028-62532315
企業郵箱:shibeikang@sbkswyy.cn
公司地址:成都市高新區天宇路2号天府創意産業園25-1-1


友情鍊接