
發布時間:2018-10-31 來源: 浏覽量:6次
8月20日,FibroGen和阿斯利康聯合開(kāi)發的全球首款、中(zhōng)國首發新藥羅沙司他(商(shāng)品名:愛瑞卓 )在中(zhōng)國收獲全球第二個适應症,即非透析的慢(màn)性腎性貧血(NDD-CKD)。
)在中(zhōng)國收獲全球第二個适應症,即非透析的慢(màn)性腎性貧血(NDD-CKD)。
即非透析的慢(màn)性腎性貧血(NDD-CKD)。
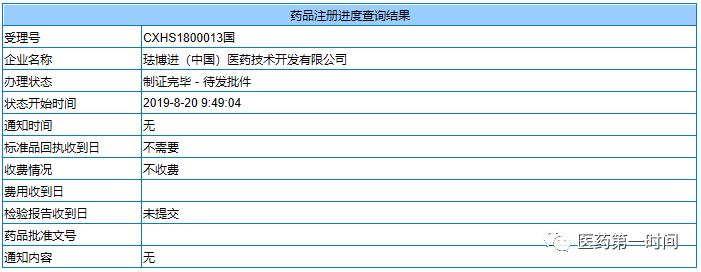
羅沙司他是全球首個口服低氧誘導因子脯氨酰羟化酶抑制劑(HIF-PHI),于2018年12月17日獲國家藥監局批準上市,用于慢(màn)性腎 髒病(CKD)透析患者貧血的治療,包括血液透析和腹膜透析患者。值得一(yī)提的是,羅沙司他是首次由中(zhōng)國首先批準全新作用機制的國際首創原研藥上市,實現了三“首”的創新突破。
羅沙司他在中(zhōng)國适應症開(kāi)發領先于全球,此次非透析的慢(màn)性腎性貧血适應症也是率先中(zhōng)國獲批。截至目前,羅沙司他日本處于上市審評階段,适應症慢(màn)性腎病透析患者貧血;歐美尚未遞交上市申請。
羅沙司他權益歸屬:
羅沙司他由FibroGen原研開(kāi)發;
2006年4月28日,FibroGen和Astellas Pharma達成羅沙司他合作開(kāi)發協議,Astellas Pharma獲得在歐洲、獨聯體(tǐ)國家、中(zhōng)東和南(nán)非地區的開(kāi)發商(shāng)業化權益;
2013年7月31日,FibroGen和阿斯利康達成羅沙司他合作開(kāi)發協議,雙方将共同在美國、中(zhōng)國以及除2中(zhōng)的世界其他地區開(kāi)發羅沙司他。
2019年,羅沙司他其他值得關注的裡程碑事件包括:
2019年第3季度,将會向FDA遞交上市申請,适應症為慢(màn)性腎病透析患者貧血或非透析的腎性貧血(DD/NDD-CKD);
2019年,将會向EMA遞交上市申請,适應症為DD/NDD-CKD;
預計在2019年第3季度中(zhōng)國正式上市;
本文主要關注支持羅沙司他此次适應症拓展的關鍵臨床試驗FGCL-4592-808 (CTR20150609, NCT02652819),同時會簡單盤點國内HIF-PH靶點抑制劑的同類産品。
一(yī).慢(màn)性腎病透析患者貧血帶來顯著臨床獲益
羅沙司他在中(zhōng)國登記有3項關鍵臨床試驗信息,彙總如下(xià)表:
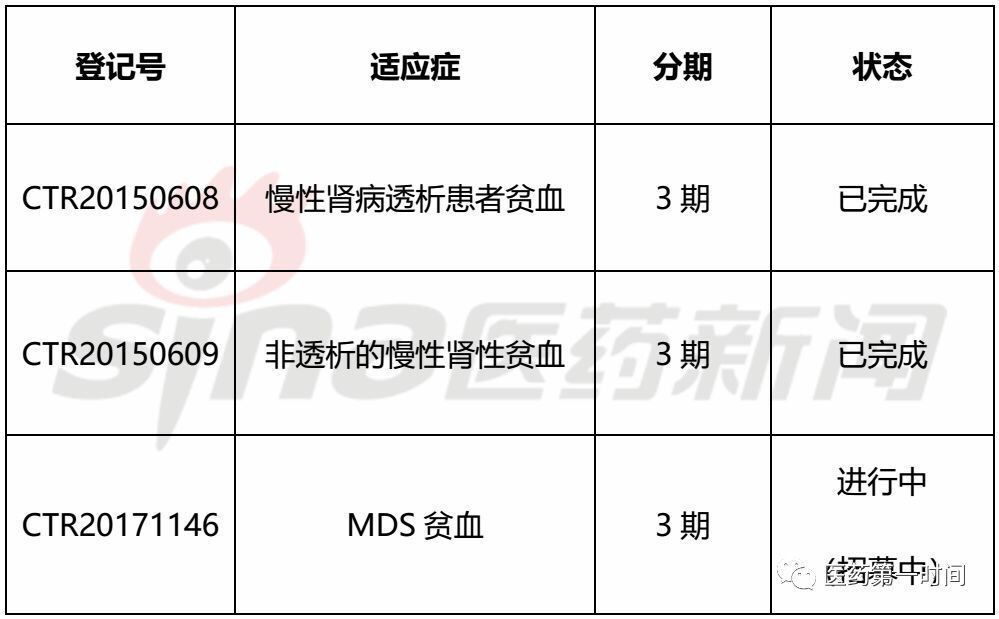
羅沙司他在中(zhōng)國登記有3項關鍵臨床試驗信息,彙總如下(xià)表:
其中(zhōng)臨床試驗FGCL-4592-808 (CTR20150609, NCT02652819) 是支持此次适應症拓展的關鍵數據,結果已經發表于新英格蘭醫學,Roxadustat for Anemia in Patients with Kidney Disease Not Receiving Dialysis.
貧血是CKD患者常見并發症之一(yī),CTR20150609共計招募患者154例,評估羅沙司他治療未接受透析的慢(màn)性腎病受試者貧血的有效性和安全性。
評估羅沙司他治療未接受透析的慢(màn)性腎病受試者貧血的有效性和安全性。
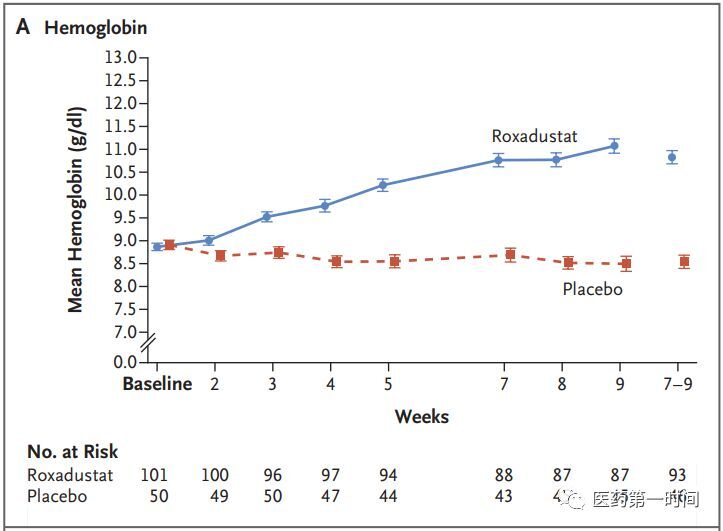
數據顯示:
羅沙司他vs.安慰劑,患者血紅蛋白(bái)水平1.9 ± 1.2 g/dL vs. -0.4±0.8 g/dL;
羅沙司他相比安慰劑,能夠顯著提高(P<0.001) 患者血紅蛋白(bái)水平,給未接受透析的慢(màn)性腎病患者帶來顯著的臨床獲益!
二.國内HIF-PH抑制劑開(kāi)發
目前在中(zhōng)國CKD患者人數超過1億,其中(zhōng)超過100萬患者是終末期,需要接受透析或腎移植治療,98.2%的透析患者為合并貧血,52.1%為非透析患者合并貧血,治療藥物(wù)主要是鐵劑和促紅素,主要的給藥方式均為注射。
筆者查詢信息發現,國内企業中(zhōng),恒瑞醫藥、東陽光藥和三生(shēng)制藥的HIF-PH抑制劑已經處于臨床階段或是剛剛IND, 主要信息如下(xià):
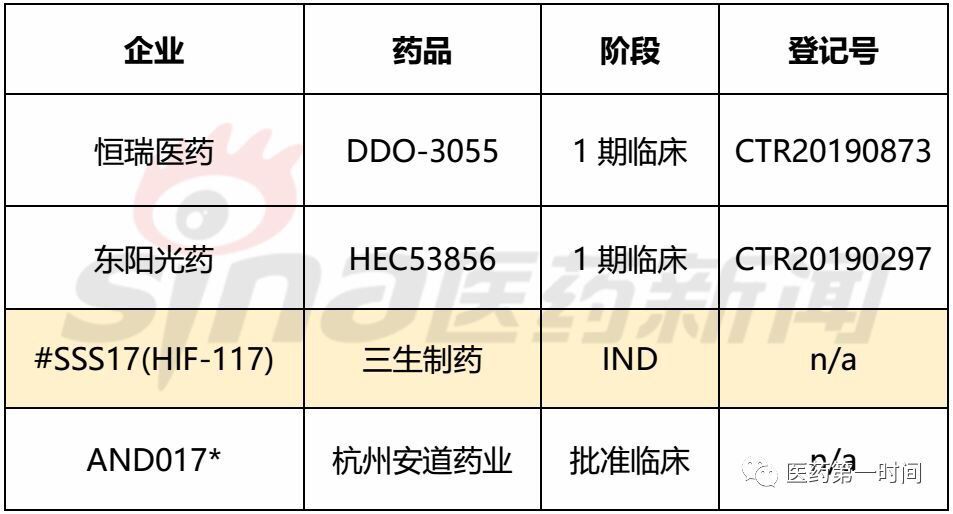
羅沙司他的潛在市場很大(dà),科睿唯安曾預測該産品在2022年的銷售額将達20億美元,EvalutePharma分(fēn)析師認為本品的銷售峰值可達58-81億美元。目前國内企業開(kāi)發的産品仍處于臨床早期,仍需長期關注相關産品開(kāi)發。
聯系我(wǒ)(wǒ)們
服務熱線:028-87988946 、028-62532315
企業郵箱:shibeikang@sbkswyy.cn
公司地址:成都市高新區天宇路2号天府創意産業園25-1-1


友情鍊接